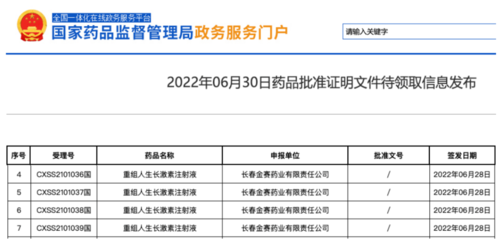
近日,金赛药业申报的重组人生长激素注射液新适应症(包括Prader-Willi 综合征)上市申请已获得国家药品监督管理局(NMPA)正式批准(受理号:CXSS2101036、CXSS2101037、CXSS2101038、CXSS2101039),这也是国内生长激素产品首次获批Prader-Willi 综合征(PWS)适应症。
多适应症获批
本次审批在此前多项获批的适应症上新加了PWS适应症,至此,金赛药业重组人生长激素注射液适应症已扩展至10个:
· 用于因内源性生长激素缺乏所引起的儿童生长缓慢;
· 用于因 Noonan 综合征所引起的儿童身材矮小;
· 用于因 SHOX 基因缺陷所引起的儿童身材矮小或生长障碍;
· 用于因软骨发育不全所引起的儿童身材矮小;
· 用于性腺发育不全(特纳综合征)所致女孩的生长障碍;
· 用于Prader-Willi 综合征(PWS);
· 用于接受营养支持的成人短肠综合征;
· 用于已明确的下丘脑-垂体疾病所致的生长激素缺乏症和经两种不同的生长激素刺激试验确诊的生长激素显著缺乏;
· 用于重度烧伤治疗;
· 用于小于胎龄儿(SGA)所引起的身材矮小。
关于Prader-Willi 综合征
PWS又称肌张力低下-智能障碍-性腺发育滞后-肥胖综合征,俗称小胖威利综合征,是一种基因组印记的疾病。据国际流行病学数据统计,PWS的发病率在1/10,000到1/30,000之间[1]。目前,40~100%的PWS患者因生长激素缺乏导致身材矮小,而国内外已有临床试验及临床指南提出,重组人生长激素治疗PWS患者具有多方面的获益,如身高、瘦体重、运动、行为、认知等方面[2-3]。而早在 2000 年,美国FDA已批准重组人生长激素用于治疗PWS儿童矮小。
参考文献:
1. Cassidy, S. B. Genet Med 2012; 14(1): 10-26
2. Genet Med. 2018 January ; 20(1): 24–30
3. J Clin Endocrinol Metab, June 2013,98(6):E1072-87
声明:本网转发此文章,旨在为读者提供更多信息资讯,所涉内容不构成投资、消费建议。文章事实如有疑问,请与有关方核实,文章观点非本网观点,仅供读者参考。
 精彩推荐
精彩推荐
 每周热点
每周热点










